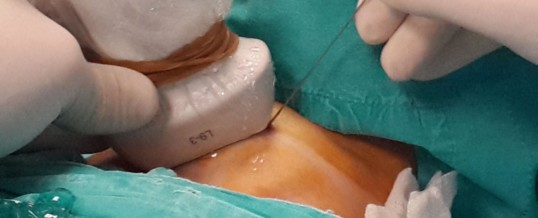
AGOASPIRATO TIROIDEO
L’ agoaspirato tiroideo (Fine Needle Aspiration, FNA) è una metodica minimamente invasiva che consente, nella maggior parte dei casi, una diagnosi precisa sulla natura dei noduli della tiroide.
Tale metodica, nel caso di voluminose cisti (colloidali o emorragiche), può avere anche una valenza terapeutica.
Il razionale dell’agoaspirato tiroideo consiste nel prelevare alcune cellule tiroidee (tireociti) contenute nel nodulo che si vuole analizzare al fine di ottenere informazioni precise sulla natura del nodulo tiroideo. L’ultima frontiera è l’agoaspirato micro-istologico con matrice, una procedura innovativa che consente una maggiore diagnosticità e permette di evitare successive ripetizioni dell’agoaspirato (Prenota un agoaspirato tiroideo).
TECNICA
L’ agoaspirato tiroideo è una metodica minimamente invasiva che consente solo il prelievo di alcune cellule contenute nel nodulo e non di un intero tessuto e pertanto non è una biopsia. Di conseguenza l’analisi del materiale prelevato sarà di tipo citologico e non istologico.
Esistono diverse tecniche con cui può essere effettuato; tuttavia l’esecuzione dell’agoaspirato tiroideo prevede sempre l’utilizzo di un ago sottile (calibro di 20-24 G) che può essere attaccato ad una siringa (quando si effettui la tecnica di aspirazione) o non attaccato ad una siringa (nel caso si effettui un prelievo per capillarità).
Il prelievo, in base alla quantità dei materiale che viene prelevato, dura solitamente solo pochi secondi e data la mini-invasività solitamente non richiede mai l’anestesia locale.
Solitamente, e soprattutto per i noduli più piccoli, l’agoaspirato viene effettuato sotto guida ecografica. La guida ecografia consente: a) di prelevare cellule anche da noduli clinicamente non palpabili e quindi non altrimenti esaminabili; b) di scegliere, in base alle caratteristiche ecografiche, quale nodulo o quale parte di nodulo agoaspirare; c) di aumentare il potere diagnostico dell’agoaspirato. (Prenota un’ecografia tiroidea).
Una volta effettuato il prelievo si passa all’allestimento del materiale. Lo striscio diretto su vetrino rappresenta tuttora la tecnica più diffusa, perché rapida, poco costosa e ampiamente codificata. In alternativa il prelievo può essere inserito in un contenitore con soluzione a base di metanolo e quindi centrifugato, emolizzato e trasferito su strato sottile da parte di un sistema automatizzato; tale metodica riduce gli errori legati all’allestimento dei vetrini ma è più costosa, non consente di valutare appieno l’architettura cellulare e le caratteristiche della colloide. Infine, i campioni citologici possono essere immersi in fissativo e processati mediante inclusione in paraffina. Poiché i dettagli citomorfologici appaiono differenti rispetto a quelli tradizionalmente codificati per gli strisci su vetrino, la tecnica del cell-block non sostituisce ma piuttosto è complementare agli strisci citologici offrendo una risorsa per possibili indagini immunocitochimiche o molecolari. (Prenota una visita endocrinologica).
INDICAZIONI
L’esame citologico mediante agoaspirazione rappresenta attualmente il gold standard nella gestione diagnostica del nodulo tiroideo.
Tuttavia, l’elevata prevalenza della patologia nodulare nella popolazione e la frequenza con cui i noduli tiroidei vengono diagnosticati incidentalmente richiedono precisi criteri per la selezione delle lesioni da sottoporre all’indagine.
Le attuali indicazioni ad eseguire un agoaspirato tiroideo sono:
– noduli palpabili in accrescimento progressivo;
– noduli di diametro inferiore a 10 mm che presentino uno o più caratteristiche ecografiche di sospetto (ipoecogenicità, margini irregolari, vascolarizzazione intralesionale e presenza di microcalcificazioni); (prenota un’ecografia tiroidea).
– noduli in soggetti ad alto rischio (familiarità per MEN o carcinoma midollare familiare, carcinoma papillare familiare, anamnesi personale di neoplasia della tiroide, pregressa irradiazione tiroidea).
EFFETTI COLLATERALI
L’ agoaspirato tiroideo è una metodica nel complesso di semplice esecuzione e a basso costo, eseguita in regime ambulatoriale virtualmente è esente da complicazioni (la più frequente è rappresentata dalla formazione di un ematoma a livello della zona di aspirazione, che può essere prevenuta dall’applicazione di ghiaccio per alcuni minuti).
E’ una tecnica la cui percentuale di successo dipende in larga misura dall’esperienza dell’operatore e da quella del citopatologo, dal numero di campioni prelevati e dai criteri utilizzati per definire l’adeguatezza del campione. E’ diventata pratica comune, soprattutto in Europa, l’esecuzione dell’ agoaspirato tiroideo sotto guida ecografica. Tale approccio permette di centrare meglio l’area da agobiopsiare, di controllare che durante l’aspirazione l’ago non si sposti dal bersaglio e, soprattutto, permette di decidere quale nodulo biopsiare in base non solo alle dimensioni, ma anche alle sue caratteristiche ecografiche. (Prenota un agoaspirato tiroideo).
RISULTATI
Le linee guida della AACE raccomandano di eseguire l’ agoaspirato tiroideo su tutti i noduli accessibili, non solo su quello di maggiori dimensioni e raccomandano altresì che l’esame venga eseguito dall’endocrinologo quale maggiore esperto nella valutazione delle caratteristiche dei noduli tiroidei. Le percentuali di agoaspirati adeguati per la diagnosi sono abbastanza sovrapponibili nelle varie casistiche e si aggirano intorno all’80%. Tale percentuale sale fino al 90% nel caso in cui l’agoaspirato è stato eseguito con guida ecografica. L’esame può essere eseguito a mano libera oppure utilizzando guide inserite sulla sonda ecografica. In caso di campioni non diagnostici la ripetizione dell’esame diminuisce la percentuale dei falsi negativi. (Prenota un agoaspirato tiroideo).
CLASSI DIAGNOSTICHE
Lo scopo principale dell’ agoapsirato tiroideo è distinguere i pazienti che devono essere sottoposti a trattamento chirurgico per il loro alto rischio di malignità da quelli che possono essere seguiti nel tempo perché a rischio molto basso. Pertanto, il referto citologico dovrebbe essere descrittivo ma anche concludersi con l’attribuzione del paziente ad una categoria diagnostica ben definita ed identificabile con un codice numerico. Attualmente viene al momento raccomandato ai citopatologi e agli endocrinologi italiani l’impiego della Classificazione della Società Italiana di Anatomia Patologica e Citopatologia Diagnostica (SIAPEC) che prevedeva le seguenti cinque categorie:
Tir 1. Non diagnostico. Ripetere la manovra, a meno che la lesione non sia rappresentata da una cisti pura. Ove possibile, attendere almeno un mese.
Tir 2. Benigno. Follow-up clinico-ecografico. Ripetere la FNA in caso di lesioni sospette all’ecografia, in accrescimento dimensionale o a giudizio del clinico e del citopatologo.
Tir 3. Lesione follicolare. Asportazione chirurgica nella maggioranza dei casi. Considerare il follow-up solo nelle lesioni di piccole dimensioni prive di caratteri di sospetto ad una valutazione multidisciplinare. Esame estemporaneo non raccomandato.
Tir 4. Sospetto. Exeresi chirurgica. Ripetere l’ agoaspirato tiroideo solo se necessario ulteriore materiale per tecniche ancillari. Esame estemporaneo raccomandato.
Tir 5. Maligno. Chirurgia nel carcinoma differenziato. Ulteriori accertamenti in caso di linfoma, lesioni metastatiche o carcinoma anaplastico.
– Gli strisci non diagnostici (TIR 1) rappresentano nelle varie casistiche circa il 10-20% degli agoaspirati: sono caratterizzati dalla scarsità di tireociti, provocata da errori di prelievo (inesperienza dell’operatore, contaminazione ematica, campionamento inadeguato) o di processazione del campione (striscio mal eseguito, ritardata o inadeguata fissazione, difetti di colorazione). Viene considerato adeguato un campione correttamente strisciato, fissato e colorato che contenga almeno sei gruppi costituiti da 10 cellule epiteliali ben conservate. Sono spesso inadeguati i campioni derivanti da noduli cistici, che contengono liquido e cellule schiumose in degenerazione. In caso di prelievo inadeguato è opportuno ripetere la FNA sotto guida ecografica, prelevando il materiale dalle aree solide delle lesioni complesse e dalla parete delle lesioni cistiche e – nel caso di lesioni ipervascolari, ove è alto il rischio di contaminazione ematica – utilizzando aghi di calibro ridotto (es. 27 G) e minimizzando la suzione ed il traumatismo della manovra.
– La diagnosi citologica di benignità (TIR 2) rappresenta il 60-75% dei risultati: corrisponde, sul piano istologico, a noduli colloidi o iperplastici, tiroidite linfocitaria, tiroidite granulomatosa e cisti benigne. È consigliato il follow-up clinico-ecografico. Ripetere la FNA solo in caso lesioni con caratteri di sospetto alla ecografia, in caso di accrescimento del nodulo o qualora si voglia minimizzare il rischio di falsi negativi.
– La diagnosi di lesione follicolare (TIR 3) corrisponde al 15-20% delle FNA: gli strisci sono caratterizzati da colloide poco rappresentata o assente, cellule tiroidee spesso riunite in microfollicoli, talora cellule di Hürthle. Questa categoria comprende noduli iperplastici benigni, adenomi follicolari, carcinomi papillari varietà follicolare e carcinomi follicolari. In considerazione della non trascurabile probabilità di neoplasia (15-25%) è indicato l’intervento chirurgico. In una minoranza dei casi i pazienti senza caratteri clinici ed ecografici di sospetto possono essere strettamente seguiti nel tempo. Valuta il profilo di rischio del tuo nodulo TIR3. L’esame istologico estemporaneo non è raccomandato. Ultimamente Afirma, una nuova e promettente tecnica di profilazione genica, sambra fornire risultati ottimi in termini di valore predittivo negativo, indicando la natura benigna di un nodulo con relativa certezza, senza ricorrere all’intervento. Per ulteriori info: Afirma. (Prenota una visita endocrinologica). Maggiori informazioni su tutte le metodiche di genetica molecolare disponibili.
– La diagnosi di sospetto (TIR 4) comprende lesioni con caratteri citologici che suggeriscono ma non mostrano in modo decisivo caratteri di malignità. Comprende inoltre campioni con caratteri fortemente indiziari di malignità ma con cellularità insufficiente. L’indicazione è chirurgica, preceduta dalla ripetizione della FNA solo se occorre ulteriore materiale per una più adeguata definizione diagnostica (quale l’immunocitochimica o la citometria a flusso). L’esame estemporaneo intraoperatorio è raccomandato.
– La diagnosi di malignità (TIR 5) rappresenta circa il 5% degli agoaspirati: comprende carcinoma papillare, carcinoma midollare, carcinoma anaplastico, linfomi e metastasi. È raccomandata l’exeresi chirurgica per i carcinomi differenziati, pianificata sulla base dei dati clinici e strumentali. Il carcinoma anaplastico, il linfoma e le lesioni metastatiche necessitano di un ulteriore inquadramento prima della eventuale opzione chirurgica. (Prenota una visita chirurgica).
Lo studio citologico può essere integrato dall’impiego di marcatori immunocitochimici e/o genetico-molecolari. Calcitonina, cromogranina A e CEA sono impiegati nel sospetto di carcinoma midollare, mentre il PTH può identificare una lesione di pertinenza paratiroidea. PTH e calcitonina possono anche essere misurati nel liquido di lavaggio dell’ago con buona attendibilità. Nel caso di lesioni neoplastiche di non agevole attribuzione diagnostica sono utilizzati marcatori specifici di tessuto epiteliale (es. citocheratina) o linfocitario. In circostanze di difficile diagnosi morfologica il marcatore è rappresentato da indici di de-differenziazione neoplastica o proliferazione cellulare (perossidasi tiroidea, galectina 3, riarrangiamenti del gene RET, mutazioni B-RAF). (Prenota l’analisi BRAF). L’impiego di queste tecniche ha un valido ruolo orientativo ma, in virtù della limitata riproducibilità dei risultati, non è attualmente raccomandato nella routine diagnostica. Valuta i pacchetti disponibili per il nodulo TIR3.
La core needle biopsy (CNB) è una biopsia tissutale ottenuta mediante ago tranciante, in genere dotato di meccanismo retrattile a molla (Tru-cut, 18-21 G). Tale metodica, effettuata solo sotto guida ecografica, non è raccomandata per la routine diagnostica ed è riservata allo studio di masse tiroidee o cervicali di probabile significato neoplastico in cui il citoaspirato sia risultato non conclusivo (come nella diagnosi differenziale tra carcinoma anaplastico, metastasi tiroidea da neoplasia occulta, linfoma o sarcoma).
Prenota una visita endocrinologica in merito a questo argomento.
Dott. Massimiliano Andrioli
Specialista in Endocrinologia e Malattie del Ricambio
Centro EndocrinologiaOggi, Roma
viale Somalia 33A, Roma
tel/fax 0686391386
cell 3337831426
Studio EndocrinologiaOggi, Lecce
via Ruffano 4, Casarano (Lecce)
tel/fax 0686391386
cell 3337831426
Bibliografia
-Bartolazzi A, Orlandi F, Saggiorato E, et al. Italian Thyroid Cancer Study Group (ITCSG). Galectin-3-expression analysis in the surgical selection of follicular thyroid nodules with indeterminate fineneedle aspiration cytology: a prospective multicentre study. Lancet Oncol 2008, 9: 543-9.
-Rago T, Di Coscio G, Basolo F, et al. Combined clinical, ultrasound and cytological features help to predict thyroid malignancy in follicular and Hürthle cell thyroid lesion: results from a series of 505 consecutive patients. Clin Endocrinol 2007, 66: 13-20.
-Jin L, Sebo TJ, Nakamura N, et al. BRAF mutation analysis in fine needle aspiration (FNA) cytology of the thyroid. Diagn Mol Pathol 2006, 15: 136-43.
-Gharib H. Changing concepts in the diagnosis and management of thyroid nodules. Endocrinol Metab Clin North Am 1997, 26: 777-800.
-Hegedus I. The thyroid nodule. N Engl J Med 2004: 351: 1764-71.
-Nguyen G, Lee MW, Ginsberg J, et al. Fine-needle aspiration of the thyroid: an overview. Cytojournal 2005, 2: 12.
-Wang HH. Reporting thyroid fine-needle aspiration: literature review and a proposal. Diagn Cytopathol 2006, 34: 67-76.
-British Thyroid Association & Royal College of Physicians. Guidelines for management of thyroid cancer. 2007
-Duick DS, Mandel SJ. Ultrasound-guided fine needle aspiration of thyroid nodules. In “Thyroid ultrasound and ultrasound-guided FNA biopsy. Baskin HJ, Duyick DS, Levine RA eds. New York, Springer Science 2008”: 97-110.
-Wiseman SM, Baliski C, Irvine R, et al. Hemithyroidectomy: the optimal initial surgical approach for individuals undergoing surgery for a cytological diagnosis of follicular neoplasm. Ann Surg Oncol 2006, 13: 425-32.
-Baloch ZW, Cibas ES, Clark DP, et al. The National Cancer Institute thyroid fine needle aspiration state of the science conference: a summation. Cytojournal 2008, 5: 6-23.
GIU
2011
