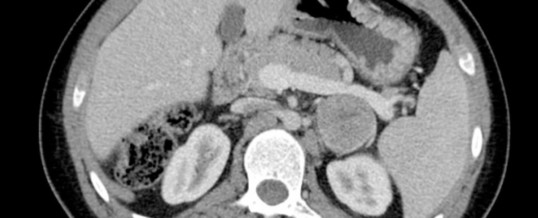
TUMORI DEL SURRENE
I tumori del surrene si differenziano dalle altre neoplasie in quanto alla componente prettamente oncologica (adenomi e carcinomi) può associarsi una componente endocrina (tumori secernenti o non secernenti).
I tumori del surrene possono originare dalla corteccia o dalla midollare del surrene.
I tumori che originano dalla corteccia surrenale possono secernere:
– cortisolo con conseguente sindrome di Cushing;
– aldosterone con conseguente morbo di Conn;
– steroidi sessuali quali testosterone o estrogeni.
I tumori derivanti dalla midollare del surrene (feocromocitoma), infine, secernono catecolamine.
TUMORI DELLA CORTECCIA DEL SURRENE
Per questi tumori è stata rivista la teoria secondo la quale i tumori benigni e maligni rappresentino due entità eziologicamente distinte; attualmente si ipotizza che l’iperplasia nodulare, l’adenoma ed il carcinoma rappresentino un continuum nell’evoluzione dello sviluppo tumorale. Secondo la teoria di Knudson dei due colpi, infatti, un tumore si sviluppa dopo una prima serie di alterazioni genetiche (evento inizializzante) cui segue la crescita di diversi gruppi cellulari. In seguito, l’instaurarsi di una seconda alterazione genetica porta alla selezione del gruppo cellulare con le migliori caratteristiche per la crescita (progressione tumorale) e quindi alla crescita incontrollata della neoplasia. Le lesioni benigne (nodulo iperplastico e/o adenoma) rappresenterebbero la prima fase ed i carcinomi la seconda fase dello sviluppo tumorale. Questa ipotesi è sostenuta, tra l’altro, dal fatto che alcuni oncogeni sono presenti già negli adenomi, benchè ad un livello di espressione nettamente inferiore a quello che si riscontra nei carcinomi. (Prenota una visita endocrinologica).
GENETICA
L’analisi dell’assetto cromosomico tumorale ha consentito di evidenziare numerose alterazioni cromosomiche, sia nei tumori surrenalici benigni che in quelli maligni. In particolare, in ¼ degli adenomi, vi è un aumento delle copie di DNA del braccio corto del cromosoma 4, mentre nei tumori maligni, oltre ad un aumento di copie nei cromosomi 4, 5, 9 e 12, vi può essere una perdita di frammenti genici sui cromosomi 1, 2 11, e 17.
Il gruppo di geni più studiati nel carcinoma surrenalico è situato sul braccio corto del cromosoma 11. In questa sede si trovano tre geni, due oncosoppressori (H19 e p57/KIP2 ) ed un fattore di crescita (IGF-II) , i quali vengono espressi o dall’allele paterno (per l’IGF-II) oppure da quello materno (per H19 e p57/KIP2) anzichè da entrambi gli alleli come avviene normalmente per i geni autosomici. Queste alterazioni vengono utilizzate per confermare la diagnosi di carcinoma, e sono utili nella pratica clinica in quanto i livelli intratumorali di IGF-II costituiscono un fattore predittivo di recidiva.
Un altro gene coinvolto nella genesi dei tumori surrenalici è il p53 (proteina oncosoppressiva), spesso espresso da un unico allele per perdita di eterozigosità oppure mutato.
Altri fattori di crescita studiati nei tumori surrenalici sono l’EGF , il TGF alfa ed il VEGF (vascular endothelial growth factor).
Un’alterazione genetica con chiaro nesso causale è stata dimostrata per l’iperaldosteronismo familiare tipo 1. In questa forma ereditaria, il gene che porta alla sintesi di aldosterone (aldosterone sintetasi) viene a trovarsi sotto il controllo del promotore del gene per la 11ßidrossilasi. A causa del carattere ibrido di questo gene, la secrezione di aldosterone viene controllata dall’ACTH, anzichè dall’angiotensina come avviene normalmente. Questi casi possono beneficiare del trattamento con desametasone.
Causale è anche la presenza di recettori aberranti, ossia espressi in sedi improprie oppure sovraespressi sulla corteccia surrenalica. Tra questi sono stati dimostrati i recettori per il GIP (gastric inhibitory peptide), il glucagone, le catecolamine, la serotonina, le gonadotropine, il TRH, la vasopressina, la leptina e l’interleuchina-1. Ciò può portare alla secrezione di cortisolo dopo stimoli quali il pasto, la postura eretta e la somministrazione di agonisti beta adrenergici e serotoninergici, di gonadotropine, TRH, o vasopressina. Questi recettori sono stati inizialmente identificati nelle iperplasie nodulari dei pazienti con questo tipo di sindrome di Cushing, ma attualmente si ritiene che essi siano presenti anche in una parte di adenomi secernenti cortisolo e negli incidentalomi. (Prenota una visita endocrinologica).
E’ stato recentemente osservato che il frammento aminoterminale della proopiomelanocortina (POMC) esplica una attività proliferativa sulle cellule del corticosurrene ed, al tempo stesso, inibisce la steroidogenesi.
Infine, un’alterazione genetica con chiare implicazioni sulla terapia dei tumori maligni è il riscontro del gene MDR1 (multidrug resistance 1) che codifica per la glicoproteina-p, una proteina di membrana che favorisce l’uscita di farmaci dalla cellula. Questa proteina è sovraespressa nei tumori surrenalici maligni e ciò verosimilmente contribuisce alla scarsa efficacia dei farmaci antiblastici.
Va infine ricordato che l’analisi genetica del tessuto tumorale è resa incerta dal diverso assetto genetico che può essere presente in zone differenti del tumore.
ESAMI DI LABORATORIO
1) Tumori secernenti cortisolo
La produzione di cortisolo in eccesso da parte del surrene determina il quadro noto come sindrome di Cushing non ACTH dipendente.
La presentazione clinica della sindrome di Cushing è differente a seconda che la causa sia un adenoma, un’iperplasia nodulare oppure un carcinoma surrenalico. Nelle prime due forme, infatti, la sintomatologia ha insorgenza graduale, anche nell’arco di diversi anni, ed è spesso sfumata. Nei pazienti affetti da carcinoma surrenalico, invece, si sviluppa in genere un quadro clinico di ipercortisolismo franco in un arco di tempo relativamente breve, di circa un anno. Il sospetto clinico, inoltre, viene supportato dagli esami di laboratorio che sono chiaramente indicativi di ipercortisolismo nel carcinoma surrenalico mentre possono essere necessarie indagini ripetute per formulare la diagnosi di sindrome di Cushing da adenoma surrenalico o iperplasia nodulare.
Gli esami di laboratorio utilizzati per la diagnosi di sindrome di Cushing non ACTH dipendente sono costituiti dalla misurazione del cortisolo libero urinario delle 24 ore (almeno 3 raccolte data l’episodicità della secrezione di cortisolo), dalla determinazione del ritmo circadiano del cortisolo (misurazione del cortisolo plasmatico oppure salivare alla mezzanotte) e dal test di soppressione con desametasone a basse dosi (Test di Nugent: 1 mg alle ore 23 con misurazione del cortisolo plasmatico il mattino seguente). Se questi esami sono indicativi di ipercortisolismo endogeno, si procede alla determinazione dei livelli plasmatici di ACTH. Il riscontro di valori di ACTH indosabili oppure dosabili ma più bassi del limite inferiore della norma è chiaramente indicativo di una forma surrenalica. Talora, tuttavia, le concentrazioni di ACTH risultano comprese nel range di norma e può essere necessario effettuare il test al CRH per escludere la presenza di una malattia di Cushing. (Prenota una visita endocrinologica).
Nel sospetto di un’iperplasia surrenalica nodulare andranno eseguiti diversi test di stimolo (farmaci serotoninergici, pasto, stazione eretta, GnRH) per svelare la presenza di recettori aberranti. Questo dato, oltre che di interesse diagnostico, può anche consentire una terapia farmacologica specifica.
2) Tumori secernenti aldosterone
La produzione di aldosterone in eccesso da parte del surrene determina il quadro noto come iperaldosteronismo. Nel caso in cui l’iperaldosteronismo sia causato da un adenoma si parla di morbo di Conn.
La diagnosi di iperaldosteronismo primario riveste notevole importanza in quanto si ritiene oggi che il 5-10% dei casi di ipertensione arteriosa sia sostenuto da questa patologia (Prenota una visita cardiologica). I criteri diagnostici sono peraltro ancora dibattuti sia per quanto riguarda i test di screening (rapporto aldosterone/attività reninica plasmatica, test al captopril, carico salino) che di diagnosi. E’ opportuno, inoltre, distinguere tra forme monolaterali e bilaterali per stabilire il corretto approccio terapeutico. Tuttavia, nessuno dei test proposti presenta un’accuratezza diagnostica assoluta.
Particolarmente discusso è l’impiego del rapporto aldosterone/attività reninica plasmatica per lo screening dei pazienti ipertesi. Infatti, il valore discriminante adottato da vari autori per identificare i pazienti affetti da iperaldosteronismo varia da 25 a 45. La variabilità di questo rapporto è presumiblmente legata alle oscillazioni della secrezione di aldosterone e renina così come all’influenza di alcuni polimorfismi, come quelli del gene per la aldosterone sintetasi (CYP11B2). In ogni caso, quello dell’ortostatismo è oggi considerato il miglior test diagnostico: un rapporto aldosterone/attività reninica di 40 ha infatti un’ottima sensibilità (100%) e una specificità dell’84%. Se viene assicurata un’elevata assunzione di sodio con la dieta nei quattro giorni precedenti, il test non ha solo valore di screening ma anche di conferma. Nel test al captopril o agli inibitori del recettore dell’angiotensina risulta diagnostico un rapporto aldosterone/attività reninica > 20 (sensibilità 80%, specificità 90%).
Le dimensioni generalmente piccole del tumore non consentono talora di stabilire con certezza un’origine monolaterale dell’iperaldosteronismo, per cui può essere necessario ricorrere al cateterismo venoso surrenalico bilaterale, con o senza stimolazione con ACTH. (Prenota una visita endocrinologica).
3)Tumori secernenti ormoni sessuali
Questi tumori sono molto rari e vanno sospettati nel caso di pseudopubertà precoce maschile, pseudoermafroditismo femminile, o in presenza di segni di virilizzazione insorti repentinamente in una donna di età adulta o avanzata. La diagnosi di questi tumori viene effettuata mediante il dosaggio dei livelli plasmatici di testosterone e degli altri androgeni (androstenedione, DHEA e DHEA-solfato) che si riveleranno elevati. Va ricordato, tuttavia, che in donne affette da policistosi ovarica o in menopausa, le concentrazioni di testosterone possono essere moderatamente elevate. La diagnosi differenziale con i tumori ovarici secernenti verrà effettuata attraverso l’indagine radiologica (ecografia pelvica e addominale, TAC o RMN) oppure, nel dubbio di tumore molto piccolo, con l’ausilio della scintigrafia con iodometil-norcolesterolo. Tumori surrenalici secernenti estrogeni o progesterone sono estremamente rari.
ESAMI STRUMENTALI
In questo campo sono stati fatti notevoli progressi sia per la valutazione funzionale della neoplasia che per la stadiazione e il follow-up delle forme maligne.
L’indagine radiologica iniziale è la TAC che identifica la sede e l’estensione della lesione. Una prima distinzione tra lesione benigna/maligna e lesione corticale/midollare può essere effettuata mediante la quantificazione delle Hounsfield Units: valori <10 HU identificano tessuti ad alta densità lipidica e pertanto escludono il feocromocitoma e le metastasi. In questo contesto, la RMN non sembra essere superiore alla TAC, mentre il suo impiego viene riservato alla biopsia guidata delle lesioni surrenaliche nel caso di sospetto secondarismo in pazienti oncologici.
Normalmente, la scintigrafia con norcolesterolo marcato con iodio 131 o selenio 75 identifica il tessuto corticosurrenale secernente e pertanto consente di stabilire se una lesione surrenalica è funzionante. Questa scintigrafia è attualmente impiegata nella diagnosi differenziale tra adenoma e iperplasia nodulare (nel primo caso si avrà una captazione omolaterale alla massa, nel secondo una captazione bilaterale) se la TAC non risulta sufficientemente informativa. Per quanto concerne la distinzione tra lesioni benigne e maligne viene attualmente suggerita la PET utilizzando il 18F-fluorodesossiglucosio quale tracciante: una forte captazione in sede surrenalica o in altre sedi, consente infatti di identificare le lesioni maligne primitive o secondarie indipendentemente dal loro stato secretorio. Tuttavia, alcuni feocromocitomi benigni possono risultare positivi alla PET e ciò limita il potenziale diagnostico dell’indagine, a meno di poter escludere a priori un feocromocitoma. Un tracciante più specifico per il surrene, il 11C-metomidato (un inibitore della 11ßidrossilasi), consente infine di effettuare una stadiazione della lesione e identificare eventuali metastasi e recidive.
TERAPIA CHIRURGICA
L’avvento della surrenalectomia per via laparoscopica, nel 1992, ha costituito una svolta per la rimozione chirurgica dei tumori surrenalici, in precedenza gravata da una mortalità perioperatoria del 4%. La surrenalectomia laparoscopica, per contro, presenta una mortalità e morbidità molto contenuta, salvo nei pazienti affetti da morbo di Conn nei quali vi può essere una compromissione cardiovascolare. La rimozione per via laparoscopica viene attualmente consigliata per tutte le lesioni surrenaliche di diametro inferiore a 6 cm (secondo alcuni, possono essere rimosse per via laparoscopica anche lesioni più grandi) che non presentino segni radiologici di malignità o invasività locale e/o a distanza. Anche i carcinomi vengono attualmente operati per via laparoscopica purchè rientrino in questi criteri. (Prenota una visita chirurgica).
La rimozione della lesione porta alla remissione clinica nella quasi totalità degli adenomi surrenalici secernenti cortisolo ed in quelli secernenti ormoni sessuali, mentre solo nel 60% dei pazienti affetti da morbo di Conn si ottiene una normalizzazione dei valori pressori. Le percentuali maggiori di successo per questa patologia si osservano nei pazienti giovani (età inferiore a 50 anni), sensibili alla terapia con spironolattone e affetti da lesioni monolaterali, mentre nei pazienti più anziani o affetti da forme bilaterali è spesso preferibile limitarsi ad un controllo farmacologico della pressione arteriosa. La rimozione dell’adenoma può servire peraltro a ridurre il regime di farmaci antiipertensivi ed a migliorare i danni d’organo causati dall’attivazione continua del recettore per i mineralcorticoidi sito sulle cellule endoteliali.
Per quanto concerne i carcinomi surrenalici, l’intervento (per via laparoscopica o a cielo aperto) deve essere il più radicale possibile, anche se ciò, spesso, può risultare difficile nella maggior parte dei pazienti che vengono diagnosticati in III o IV stadio; infatti, la percentuale di sopravvivenza dei pazienti con questa neoplasia è bassa (25-30% a 5 anni).
TERAPIA MEDICA
Elementi di novità nella terapia farmacologica dei tumori surrenalici sono presenti principalmente nel campo dei carcinomi surrenalici. La rarità di questo tumore ha consentito sinora solo pochi studi su grandi casistiche. In ogni modo, la letteratura riferisce del contenimento, della regressione tumorale su piccoli gruppi di pazienti trattati con mitotane (o,p’DDD) da solo o in associazione a chemioterapici quali l’etoposide, il cisplatino, la doxorubicina o la streptozocina. Le percentuali di risposta parziale o completa non superano peraltro il 50%. Alcuni studi recenti hanno consentito di delucidare i meccanismi alla base di questa scarsa responsività: anzitutto l’effetto citotossico del mitotane richiede una sua trasformazione all’interno della cellula ed ogni tumore presenta una differente capacità di metabolizzare il farmaco. Inoltre, i carcinomi surrenalici esprimono la glicoproteina-p che, come in altri tumori, induce una resistenza ai chemioterapici. (Prenota una visita endocrinologica).
TUMORI DELLA MIDOLLARE DEL SURRENE
Come per i tumori della corteccia surrenalica, anche per i feocromocitomi non è possibile fare una chiara distinzione tra forme benigne e maligne solo su base istopatologica. Pertanto i feocromocitomi maligni vengono identificati in base all’invasività locale o a distanza, sia al momento della diagnosi che dopo un follow-up di almeno 3 anni. In generale, i feocromocitomi extrasurrenalici, quelli di grandi dimensioni e quelli con aree necrotiche al loro interno hanno maggiori probabilità di essere maligni.
GENETICA
A differenza dei tumori della corteccia surrenalica, quasi sempre sporadici, il 10-20% dei feocromocitomi ha un’origine familiare e ciò ha accelerato la ricerca dei geni responsabili. Esistono, inoltre, alcune sindromi ereditarie che comprendono nel loro quadro il feocromocitoma: tra queste la MEN2 , che vede coinvolto il protooncogene RET oltre che un locus sul braccio lungo del cromosoma 10, la sindrome di von Hippel-Lindau (VHL), il cui gene oncosoppressore è stato identificato sul braccio corto del cromosoma 3, e la malattia di von Recklinghausen o neurofibromatosi di tipo 1, conseguente ad una mutazione inattivante dell’oncosoppressore NF1 situato sul cromosoma 17. Di particolare interesse è il gene VHL, coinvolto nell’angiogenesi indotta dall’ipossia cellulare, in quanto le diverse mutazioni descritte sinora possono indurre tumori con caratteristiche differenti. Infatti, le mutazioni inattivanti danno luogo a tumori altamente vascolarizzati, le mutazioni che portano ad un’aumentata sintesi della proteina VHL inducono feocromocitomi non particolarmente vascolarizzati, una mutazione puntiforme, infine, da’ luogo ad emangioblastoma, feocromocitoma e carcinoma renale più o meno vascolarizzati a seconda dell’ipo- o iperattività della proteina VHL. Evidentemente la stessa molecola, se espressa in quantità differente, evoca processi di tumorigenesi opposti.
Uno studio recentissimo ha identificato un altro gene coinvolto nella genesi dei feocromocitomi, la succinato deidrogenasi (SDH), una flavoproteina il cui gene codificante è situato sul cromosoma 11 anch’essa coinvolta nell’angiogenesi. Una sua mutazione germinale è stata osservata in oltre il 15% dei pazienti affetti da feocromocitoma sporadico, nel 10% dei feocromocitomi familiari e in buona parte dei feocromocitomi extrasurrenalici, specie nei paragangliomi del collo e della testa. (Prenota una visita endocrinologica).
Altri fattori coinvolti nella genesi dei feocromocitomi sono il VEGF , che risulta significativamente più espresso nel tessuto midollare tumorale rispetto a quello normale, e la trascrittasi inversa delle telomerasi , quest’ultima spesso predittiva di malignità. Da segnalare ancora una elevata frequenza di iperespressione di proteina bcl-a . Infine, il cromosoma 1 presenta spesso una perdita di eterozigosità e potrebbe quindi essere un’ulteriore sede di geni candidati per il feocromocitoma.
ESAMI DI LABORATORIO
La diagnosi di feocromocitoma ha subito notevoli progressi con l’affinamento delle metodiche di dosaggio delle catecolamine e dei suoi metaboliti; in particolare, l’introduzione del dosaggio delle metanefrine plasmatiche consente di ovviare alle problematiche legate all’interferenza con farmaci e all’episodicità della secrezione di catecolamine. Questa metodica è attualmente consigliata come test di screening per il feocromocitoma in quanto offre una sensibilità e specificità vicine al 99%. La disponibilità del dosaggio delle metanefrine plasmatiche ovvia anche all’esecuzione di ulteriori test di conferma, come il test alla clonidina ed il test al glucagone, peraltro gravati da un numero cospicuo di falsi positivi e negativi.
ESAMI STRUMENTALI
TAC, RMN e scintigrafia con meta-iodobenzilguanidina (MIBG) rappresentano le indagini classiche. La scintigrafia, tuttavia, risulta spesso negativa nei paragangliomi del collo, forse per la scarsa capacità di questi tumori a sintetizzare e secernere catecolamine. Nei casi dubbi si può eseguire la scintigrafia con analoghi marcati della somatostatina (octreoscan) in quanto i feocromocitomi, così come i paragangliomi, presentano un’elevata densità di recettori per la somatostatina. In particolare, nel 90% dei feocromocitomi sono presenti recettori tipo 3 della somatostatina, localizzati nel citoplasma anzichè sulla membrana cellulare. Recettori del tipo 2 della somatostatina sono espressi più frequentemente nei feocromi extrasurrenalici. Nell’insieme, TAC e RMN consentono in genere di individuare la lesione pur non essendo sempre informative sulla sua natura; per contro, la scintigrafia con MIBG o octreoscan, benchè non molto sensibili, offrono informazioni sulle caratteristiche funzionali della lesione. Infine, è stata di recente introdotta la PET con 6-(18F)fluorodopamina che ha dato risultati promettenti nella localizzazione dei feocromocitomi extramidollari ed eventuali metastasi.
TERAPIA
Come per i tumori del corticosurrene, l’introduzione della surrenalectomia per via laparoscopica ha cambiato radicalmente le prospettive chirurgiche dei feocromocitomi. Dopo alcune perplessità iniziali sull’opportunità di operare tumori così poco manipolabili per la facilità di indurre crisi ipertensive, la rimozione del tumore per via laparoscopica si è dimostrata una tecnica sicura ed efficace specie nei pazienti con masse di dimensioni inferiori a 6 cm. In alcuni casi è anche possibile effettuare una rimozione selettiva del tumore, risparmiando la corteccia surrenalica. Indispensabile in questi pazienti un’accurata preparazione con alfa e beta bloccanti e, se necessario, altri farmaci antiipertensivi per controllare i valori pressori e garantire un adeguato volume plasmatico, in genere contratto, per evitare crisi ipotensive postoperatorie.
Una menzione particolare merita il feocromocitoma maligno, patologia gravata da una sopravvivenza mediocre (20-40% a 5 anni) nonostante la resezione radicale del tumore. Tra le terapie sperimentali proposte offrono alcune speranze la radioterapia con 131I-MIBG ad alte dosi e la chemoembolizzazione, anche se finora entrambe le tecniche non hanno prodotto risultati del tutto soddisfacenti.
Dott.ssa Francesca Pecori Giraldi
e
Dott. Massimiliano Andrioli
Specialista in Endocrinologia e Malattie del Ricambio
Centro EndocrinologiaOggi, Roma
viale Somalia 33A, Roma
tel/fax 0686391386
cell 3337831426
Studio EndocrinologiaOggi, Lecce
via Ruffano 4, Casarano (Lecce)
tel/fax 0686391386
cell 3337831426
Bibliografia
1) Koch CA, Pacak K, Chrousos GP. The molecular pathogenesis of hereditary and sporadic adrenocortical and adrenomedullary tumors. Journal of Clinical Endocrinology and Metabolism 2002; 87 (12):5367-84.
2) Lacroix A, N’Diaye N, Tremblay J, Hamet P. Ectopic and abnormal hormone receptors in adrenal Cushing’s syndrome. Endocrine Reviews 2001; 22 (1):75-100.
3) Invitti C, Pecori Giraldi F, De Martin M, Cavagnini F and The Study Group on the Hypothalamo-Pituitary-Adrenal Axis of the Italian Society of Endocrinology. Diagnosis and management of Cushing’s syndrome: results of an Italian Multicentre Study. Journal of Clinical Endocrinology and Metabolism 1999; 84 (2):440-8.
4) Young WF Jr. Minireview: Primary aldosteronism –changing concepts in diagnosis and treatment. Endocrinology 2003; 144 (6):2208-13.
5) Surrey E, de Ziegler D, Gambone JC, Judd HL. Preoperative localization of androgen-secreting tumors: clinical, endocrinologic, and radiologic evaluation of ten patients. American Journal of Obstetrics and Gynecology 1988;158 (6):1313-22.
6) Maurea S, Klain M, Mainolfi C, Ziviello M, Salvatore M. The diagnostic role of radionuclide imaging in evaluation of patients with nonhypersecreting adrenal masses. Journal of Nuclear Medicine 2001; 42 (6):884-92.
7) Harris DA, Au-Yong I, Basnyat PS, Sadler GP, Wheeler MH. Review of surgical management of aldosterone secreting tumours of the adrenal cortex. European Journal of Surgical Oncology 2003; 29 (5): 467-74.
8)Suzuki K. Laparoscopic surgery for malignant adrenal tumors. Biomedical Pharmacotherapy 2002; 56 (1):139-44.
9) Berruti A, Terzolo M, Pia A, Angeli A, Dogliotti L. Mitotane associated with etoposide, doxirubicin, and cisplatin in the treatment of advanced adrenocortical carcinoma. Italian Group for the Study of Adrenal Cancer. Cancer 1998; 83 (10):2194-200.
10) Hes FJ, Höppener JWM, Lips CJM. Phaeochromocytoma in von Hippel-Lindau disease. Journal of Clinical Endocrinology and Metabolism 2003; 88 (3):969-74.
11) Lenders JW, Pacak K, Walther MM, Linehan WM, Mannelli M, Friberg P, Keiser HR, Goldstein DS, Eisenhofer G. Biochemical diagnosis of pheochromocytoma: which test is best? Journal of the American Medical Association 2002; 284 (11):1427-34.
12) Pacak K, Eisenhofer G, Carrasquillo JA, Chen CC, Whatley M, Goldstein DS. Diagnostic localization of pheochromocytoma: the coming of age of positron emission tomography. Annals of the New York Academy of Science 2002 970 (9):170-6.
13) Cherki S, Causeret S, Lifante JC, Mabrut JY, Sin S, Berger N, Peix JL. Current management of pheochromocytoma: about 50 cases. Annales de Chirurgie 2003; 128 (4):232-6
GIU
2011
